新年伊始,鄭州大學(xué)董子鋼教授課題組在胃癌和食管癌防治領(lǐng)域連續(xù)發(fā)表三篇高水平研究成果。這些創(chuàng)新成果展現(xiàn)了課題組勇攀高峰、敢為人先的創(chuàng)新精神和嚴(yán)謹(jǐn)求實(shí)、協(xié)同合作的科研精神。研究成果將助力學(xué)校臨床醫(yī)學(xué)一流學(xué)科建設(shè),為消化系統(tǒng)腫瘤防治事業(yè)貢獻(xiàn)力量。
以“Chronic stress-induced cholesterol metabolism abnormalities promote ESCC tumorigenesis and predict neoadjuvant therapy response”為題目的研究成果發(fā)表在該領(lǐng)域頂尖期刊《Proceedings of the National Academy of Sciences, PNAS》上,該研究成功構(gòu)建了慢性壓力聯(lián)合4NQO誘導(dǎo)的食管癌小鼠模型,利用該模型的食管組織進(jìn)行蛋白質(zhì)組學(xué)測(cè)序,發(fā)現(xiàn)慢性壓力促進(jìn)食管癌發(fā)展的關(guān)鍵分子HMGB2。研究揭示慢性壓力能夠激活下丘腦-垂體-腎上腺軸,進(jìn)而刺激腎上腺釋放皮質(zhì)醇。皮質(zhì)醇進(jìn)入細(xì)胞后,結(jié)合并激活GCR,觸發(fā)GCR從細(xì)胞質(zhì)向細(xì)胞核的轉(zhuǎn)位。在細(xì)胞核內(nèi),激活的GCR特異性地結(jié)合至HMGB2的啟動(dòng)子區(qū)域,顯著增強(qiáng)HMGB2的轉(zhuǎn)錄活性。HMGB2作為轉(zhuǎn)錄調(diào)控因子,與轉(zhuǎn)錄因子SREBP1結(jié)合,共同促進(jìn)LDLR的轉(zhuǎn)錄,增強(qiáng)了LDL的攝取,導(dǎo)致膽固醇代謝紊亂,最終促進(jìn)了ESCC的進(jìn)展。該成果闡明了皮質(zhì)醇-GCR-HMGB2-LDLR軸在慢性壓力促進(jìn)ESCC發(fā)生與發(fā)展中的核心促進(jìn)效應(yīng),為探索ESCC的預(yù)防性策略及治療新途徑提供了重要的理論依據(jù)與潛在靶點(diǎn)。鄭州大學(xué)董子鋼教授和鄭州大學(xué)附屬腫瘤醫(yī)院趙四敏副教授為該文章的共同通訊作者,博士研究生王婷和王翔宇為論文的共同第一作者。該研究成果得到國家自然科學(xué)基金、河南省重大科技專項(xiàng)和中原學(xué)者項(xiàng)目資助,由鄭州大學(xué)、中美(河南)荷美爾腫瘤研究院和天健先進(jìn)生物醫(yī)學(xué)實(shí)驗(yàn)室共同完成。
文章鏈接:
https://doi.org/10.1073/pnas.2415042122
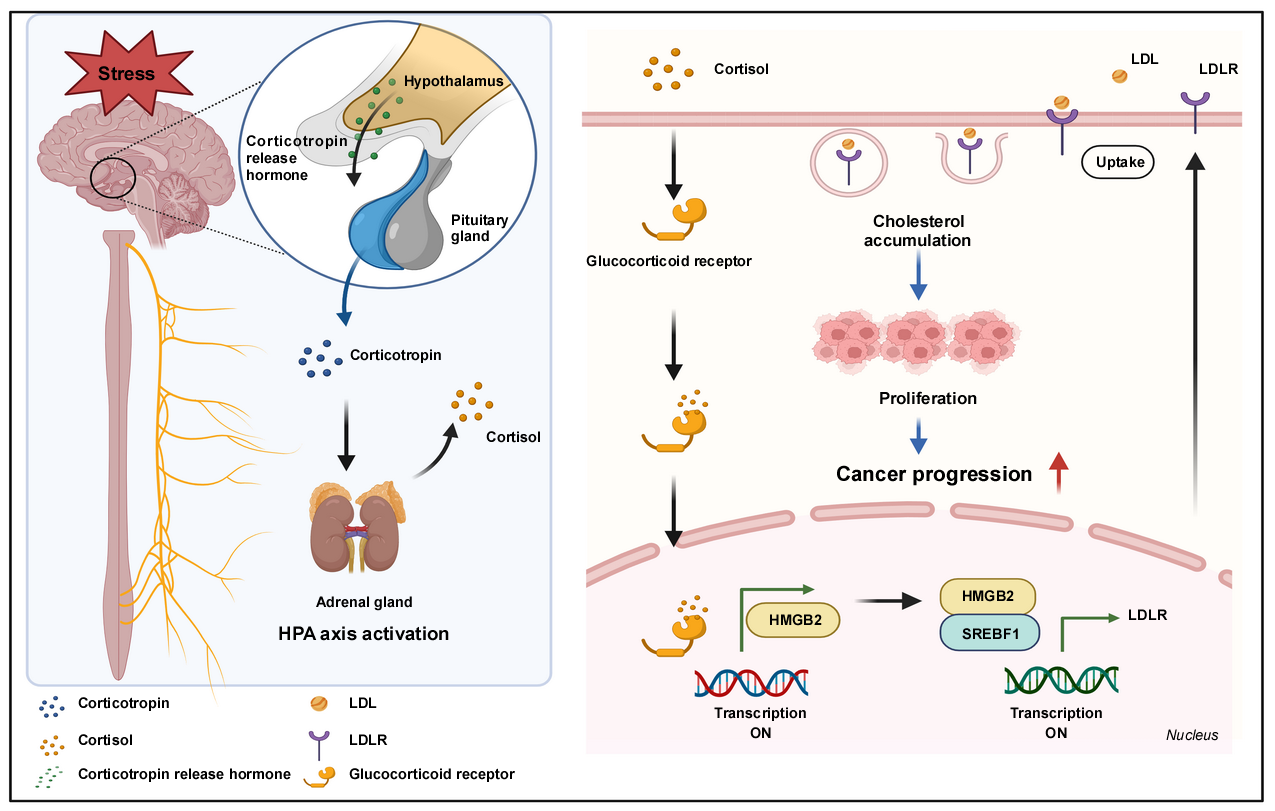 機(jī)制圖:慢性壓力通過釋放皮質(zhì)醇激活GCR-HMGB2-LDLR軸,導(dǎo)致膽固醇代謝異常,促進(jìn)ESCC的發(fā)生和發(fā)展。
機(jī)制圖:慢性壓力通過釋放皮質(zhì)醇激活GCR-HMGB2-LDLR軸,導(dǎo)致膽固醇代謝異常,促進(jìn)ESCC的發(fā)生和發(fā)展。
以“hnRNPU-mediated pathogenic alternative splicing drives gastric cancer progression ”為題目的成果發(fā)表在《J Exp Clin Cancer Res 》期刊上。該研究發(fā)現(xiàn)可變剪接事件在癌癥中廣泛發(fā)生,可能是驅(qū)動(dòng)癌癥發(fā)生的關(guān)鍵因素。通過生信分析發(fā)現(xiàn),hnRNPU是調(diào)控可變剪接事情的關(guān)鍵可變剪接因子。通過RIP-seq和MeRIP-seq分析,經(jīng)RIP和RNA pull down實(shí)驗(yàn)驗(yàn)證,發(fā)現(xiàn)hnRNPU 能夠與FTO mRNA結(jié)合,且FTO能夠調(diào)控hnRNPU的m6A甲基化修飾水平,從而增強(qiáng)hnRNPU的mRNA穩(wěn)定性。進(jìn)一步研究發(fā)現(xiàn)hnRNPU結(jié)合MET并且調(diào)控其可變剪接,致使MET穩(wěn)定性增加并持續(xù)激活進(jìn)而促進(jìn)胃癌的發(fā)生。這一研究為胃癌發(fā)生分子機(jī)制的闡明提供了重要的線索。鄭州大學(xué)董子鋼教授、郭智萍教授為文章共同通信作者,晉果果、宋延明、方少伯為文章共同第一作者。該研究成果得到國家自然科學(xué)基金和河南省重大科技專項(xiàng)項(xiàng)目資助,該研究由鄭州大學(xué),中美(河南)荷美爾腫瘤研究院和天健先進(jìn)生物醫(yī)學(xué)實(shí)驗(yàn)室共同完成。
文章鏈接:
https://jeccr.biomedcentral.com/articles/10.1186/s13046-024-03264-9

機(jī)制圖:FTO通過調(diào)節(jié)HNRNPU的甲基化水平影響MET的可變剪切促進(jìn)胃癌的發(fā)生
以“CHI-KAT8i5 suppresses ESCC tumor growth through inhibiting KAT8 mediate c-Myc stability”為題目的研究成果發(fā)表在該領(lǐng)域國際權(quán)威雜志《Cell Reports》上。該研究首先分析研究了ESCC組織中組蛋白修飾酶的表達(dá)水平,發(fā)現(xiàn)KAT8的RNA和蛋白水平都與食管鱗癌病人的預(yù)后顯著相關(guān)。KAT8的食管特異性敲除小鼠表現(xiàn)出較少的腫瘤負(fù)荷,且敲低KAT8顯著抑制CDX和PDX模型中的腫瘤生長(zhǎng)。在機(jī)制方面,該研究證實(shí)了KAT8通過直接結(jié)合c-Myc蛋白來調(diào)節(jié)c-Myc蛋白的穩(wěn)定性。此外,該團(tuán)隊(duì)設(shè)計(jì)和篩選了一種特異性KAT8抑制劑(CHI-KAT8i5),可在體內(nèi)外實(shí)驗(yàn)中顯著抑制腫瘤的生長(zhǎng),為進(jìn)一步臨床研究提供了廣闊的潛力。該研究提示KAT8可以作為 ESCC 患者的臨床相關(guān)生物標(biāo)志物和治療靶點(diǎn),CHI-KAT8i5 作為 KAT8 的有效的特異性抑制劑,是一種很有前途的可用于癌癥治療的小分子化合物。鄭州大學(xué)董子鋼教授、劉康棟教授為該文章的共同通訊作者,博士后張丹丹為論文的第一作者。該研究成果得到國家自然科學(xué)基金和河南省重大科技專項(xiàng)項(xiàng)目資助,由鄭州大學(xué)和中美(河南)荷美爾腫瘤研究院共同完成。
文章鏈接:
https://doi.org/10.1016/j.celrep.2024.115135

機(jī)制圖:CHI-KAT8i5通過抑制KAT8介導(dǎo)的c-Myc穩(wěn)定性來抑制食管鱗癌的發(fā)生發(fā)展
 移動(dòng)校園app
移動(dòng)校園app













 加入鄭大
加入鄭大 校園信息
校園信息 友情鏈接
友情鏈接

